
400-0355-662
最新消息 | 澳大利亚TGA发布了关于IVD医疗器械制造商证据的新指南
澳大利亚TGA发布了关于IVD医疗器械制造商证据的新指南

当地时间2023年6月20日,继澳大利亚主管当局(TGA)发布“Phase out of ISO 13485 certificates for IVD medical devices “的通知后,又发布了向IVD医疗器械的新制造商证据过渡的指南文件 。
本指南旨在帮助申办者和制造商过渡到体外诊断(IVD)医疗器械的新制造商证据要求。
制造商证据是提交给治疗用品管理局(TGA)的文件,通常是类似海外监管机构的监管批准证书或记录,以支持澳大利亚治疗用品注册(ARTG)中的医疗器械条目。
由于以下原因,申办者将需要新的IVD医疗器械制造商证据:
• 新的欧盟IVD法规2017/746 (EU IVDR)取代了IVD指令98/79/EC (IVDD)
• 2022年5月26日之前,TGA接受ISO 13485证书作为制造商证据的过渡期结束,除非制造商根据IVDD做出的欧盟符合性声明支持。
从TGA提供的“制造商提交的证据类型数据图”可知:
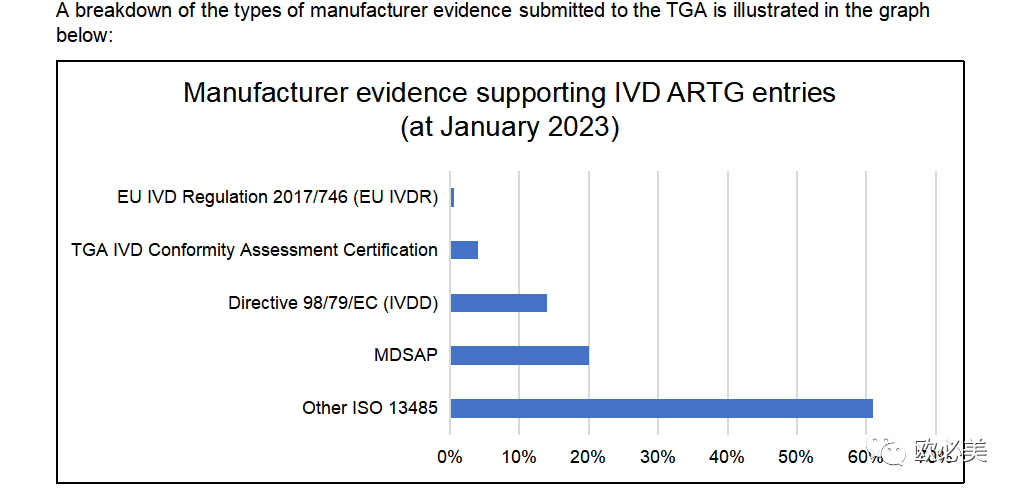
截止到2023年1月,超过60 % 的制造商选择了ISO 13485作为制造商证据来支持IVD医疗器械的纳入申请。
本指南中描述的变更也将影响约70%的IVD ARTG条目,特别是ISO 13485证书和IVDD认证支持的条目。随着时间的推移,预计这些形式的认证将主要被欧盟IVDR认证和医疗器械单一审核程序(MDSAP)认证所取代。
TGA接受不同类型的制造商证据以支持IVD医疗器械申请的截止日期总结如下。
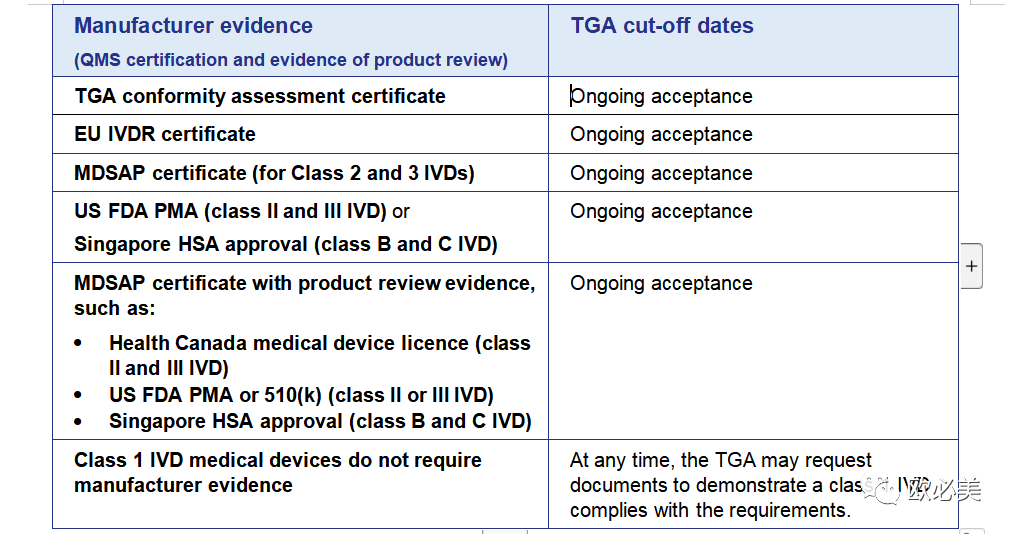
除此之外,该指南还概述了申办者在将IVD ARTG申请转换为新制造商证据时必须考虑的可能措施。
版权所有© 2023 欧必美(青岛)医疗技术有限公司 备案号:XXXX 技术支持:苏州慕名
扫描二维码分享到微信