
400-0355-662
FDA更新生物相容性指南,部分材料豁免生物相容性测试!

近日,FDA更新了生物相容性指南 Use of International Standard ISO10993-1, "Biological evaluation of medical devices - Part 1: Evaluation and testing within a risk management process"。
本指南取代2020年9月4日的“国际标准ISO10993-1的使用,“医疗器械的生物学评价-第1部分:风险管理过程中的评价和测试””。
值得注意的是该指南新增了附录G,与完整皮肤接触的某些器械的生物相容性,描述了由常见聚合物和织物制成的与完整皮肤相接触的器械推荐提交的内容。附件G建议在上市前提交中包含特定的材料信息,以代替生物相容性测试。这种方法也支持“3R”的原则,即在可行的情况下取代、减少和/或改进动物在测试中的使用。此方法基于FDA上市前提交的审查经验和质量体系法规的某些部分以及其它上市后控制。
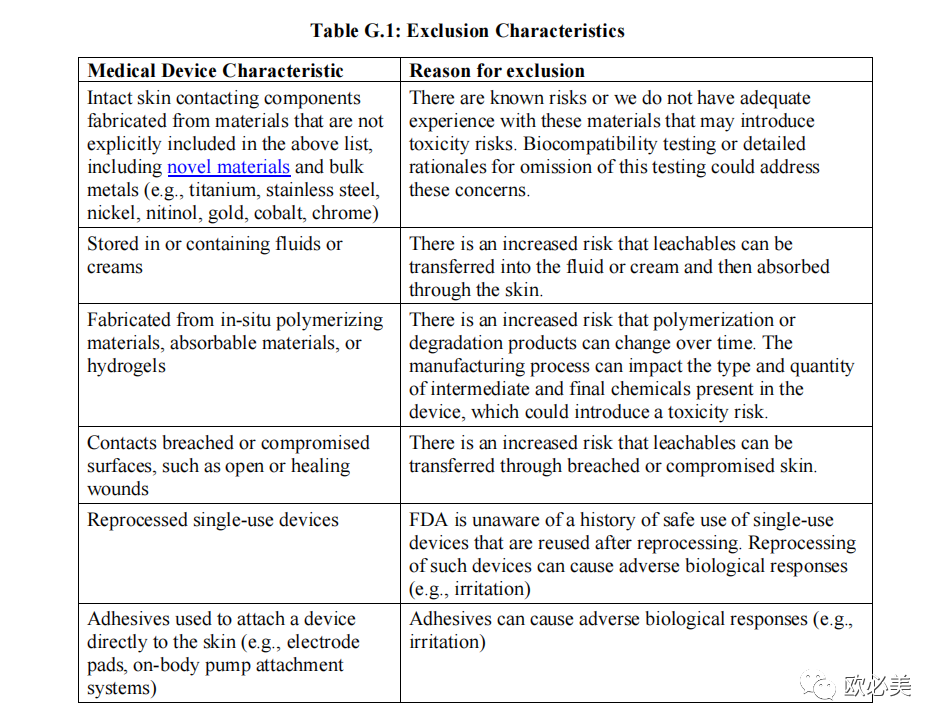
豁免生物相容性测试的设备包括哪些? 满足以下所有要求的器械可豁免生物相容性测试: 1)仅接触完整皮肤表面的医疗器械或组件; 2)接触时间可以是≤24小时、24小时-30天或者> 30天,包括重复使用设备; 3)由以下材料组成或构成的器械或部件: A. 合成聚合物 •丙烯腈-丁二烯-苯乙烯塑料(ABS); •醋酸纤维素 •固化环氧胶粘剂(用于将医疗器械组件相互连接); •含氟聚合物,包括聚四氟乙烯(PTFE)、膨胀聚四氟乙烯(ePTFE)、 聚偏氟乙烯(PVDF)和全氟(乙烯-丙烯)塑料(FEP); •丁腈橡胶(NBR); •聚对二甲苯(派瑞林); •聚酰胺(PA),如尼龙和尼龙搭扣® •聚对苯二甲酸丁二醇酯(PBT); •聚碳酸酯(PC); •氯丁,如氯丁橡胶; •聚醚酮(PEEK) •聚醚酮酮(PEKK); •聚醚嵌段酰胺(PEBA),如PEBAX®; •聚醚亚胺(PEI); •聚乙烯,包括低密度聚乙烯(LDPE)和高密度聚乙烯(HDPE); •聚对苯二甲酸乙酯(PET),如尼龙搭扣® •聚甲基丙烯酸甲酯(PMMA); •聚甲醛(POM); •聚苯砜(PPSU); •聚丙烯(PP); •聚苯乙烯(PS),包括高冲击聚苯乙烯(HIPS); •聚氨酯(PUR),如莱卡® •聚乙烯醇(PVA);或 •硅胶 B. 天然纤维 • 棉织物Cotton fabrics; • 人造丝织物Rayon fabrics; • 丝织物Silk fabrics 上市前提交的资料中应包含哪些生物相容性信息? FDA建议在附件G概述的政策范围内的设备类型的上市前提交中包含以下信息: •用于制造仅与皮肤直接或间接接触的设备或部件的所有材料(包括颜色添加剂)的清单; • 一份声明,确认器械材料属于上述材料,并有一份合法销售的医疗器械的安全使用记录(如通过医疗设备报告(MDR)分析、文献搜索); • 确认不属于下表中列出的排除情形(即,下图G.1中排除的器械)的声明;
版权所有© 2023 欧必美(青岛)医疗技术有限公司 备案号:XXXX 技术支持:苏州慕名
扫描二维码分享到微信